Развитие ребенка с пвл


В процессе родовой деятельности будущего малыша поджидает множество опасных моментов. Одним из них является перивентрикулярная лейкомаляция – патологический очаг в головном мозге новорожденного, обусловленный недостатком поступления кислорода к его клеткам.
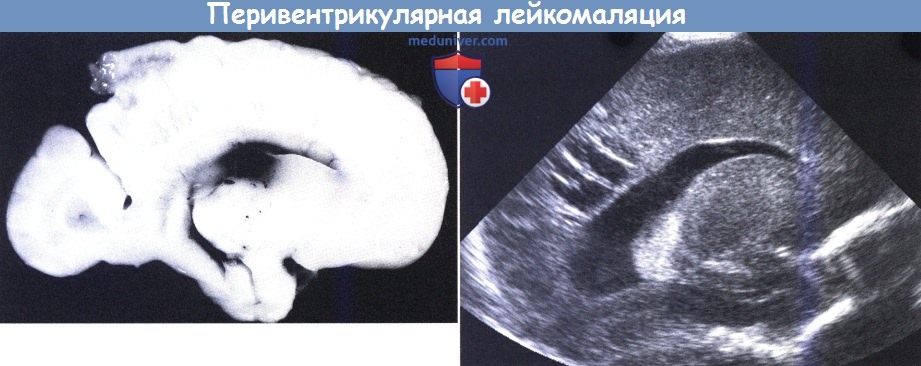
Преимущественное расположение перивентрикулярной зоны поражения – вдоль наружно-верхних отделов боковых желудочков органа. В дальнейшем они могут преобразоваться в кисты или полости, ведущие к тяжелым нарушениям центральной нервной системы малыша. Поэтому профилактике этой патологии уделяется большое внимание врачами во всем мире.
Причины и факторы риска
О важности первых 2–3 месяцев внутриутробного развития ребёнка знают большинство будущим мам. Однако последний триместр беременности также таит в себе множество опасностей для полноценного роста и формирования головного мозга человека.
Специалисты отмечают, что в особой группе риска по формированию перивентрикулярной лейкомаляции – очагам с отмирающими клетками в тканях боковых желудочков, находятся недоношенные дети и те, кто родился ранней весной.
Снижение поступления кислорода к мозговым клеткам обусловлено метеорологическими условиями, провоцирующими спазмы сосудов.

Другие факторы неврологического заболевания:
- эндокринные нарушения у будущей матери – к примеру, диабет;
- анемия беременных;
- авитаминозы;
- внутриутробное инфицирование плода;
- обильные кровотечения в момент родовой деятельности;
- резкие колебания кровяного давления у малыша;
- ранняя острая дыхательная недостаточность у новорожденного.
Тем не менее, главной причиной лейкомаляций головного мозга остается глубокая недоношенность. Поэтому основной упор акушеры-гинекологи делают на своевременную профилактику преждевременных родов и внутриутробной кислородной недостаточности.

Процесс формирования патологии
Для того чтобы понять, что такое ПВЛ и как с нею бороться, необходимо разобраться в механизме ее формирования. На фоне провоцирующих факторов в нервных клетках появляется патологический очаг – из-за кислородного голодания белое вещество органа отмирает. Полноценные нейроциты заменяются иными элементами, которые не способны выполнять те же функции.
Позже – через 7-14 суток на этом участке возникают перивентрикулярные кисты – полые или заполненные особой жидкостью. На завершающем этапе могут появляться рубцы на нервной ткани. Реже в боковых желудочках органа могут наблюдаться вторичные геморрагические инфаркты. В последующем пораженные участки полностью атрофируются.


Как правило, перивентриулярная лейкомаляция развивается в первые часы появления малыша на свет. Однако встречаются случаи, когда перивентрикулярный вариант патологии возникают позднее – до 5-7 суток от момента родов.
Поражение боковых желудочков головного мозга может происходить и внутриутробно – при беременности, сопровождающейся обострением пиелонефрита, гепатита. Для того чтобы этого избежать, женщине необходимо обращаться к наблюдающему за течением беременности врачу при первых же признаках ухудшения самочувствия.
Симптомы и признаки болезни
Заподозрить, что лейкомаляция головного мозга у новорожденных появилась, затруднительно – признаки перивентрикулярной патологии разнообразны и крайне неспецифичны. Тем не менее, недостаток поступления кислорода к нервным клеткам не протекает вовсе бессимптомно. Основные клинические признаки перивентрикулярной лейкомаляции:
- чрезмерная возбудимость новорожденного – крикливость, избыточная хаотичность движений;
- склонность к судорожным состояниям;
- вялость мышечных рефлексов.

У глубоко недоношенных детей симптоматика намного грубее:
- колебание температуры тела;
- вялость;
- повышенная сонливость;
- снижение аппетита;
- нарушение сна;
- парезы/параличи конечностей;
- дыхательные расстройства;
- зрительные нарушения – косоглазие.

Специалисты подчеркивают – проявления перивентрикулярной формы заболевания после острого периода могут стихать. Этот период мнимого благополучия длится до 8-9 месяцев. И только к году лейкомаляция головного мозга дает о себе знать дефицитом нервной деятельности. О течение патологического процесса свидетельствуют:
- недостаточная прибавка в весе;
- медленный рост;
- отставание в освоении навыков;
- несоответствие интеллекта возрасту;
- задержка психоречевого развития;
- выраженная эмоциональная лабильность.
Практически в 90% случаев это заболевание становится причиной развития детского церебрального паралича – тяжелой неврологической патологии, приводящей к инвалидизации.
Прогнозы и степень тяжести ПВЛ
Если женщине не удается доносить малыша до положенного срока – дети появляются на свет недоношенными. Родителям следует заранее подготовиться к правильному уходу за новорожденным.
Относительно благоприятным прогноз будет при легкой степени лейкомаляции головного мозга. В перивентрикулярной клинике преобладает дефицит внимания, а также гиперактивность – хаотичность движений конечностей. Тогда как моторное развитие – своевременность ползанья, ходьбы, переворотов сохраняется.

Специальные коррекционные мероприятия позволяют добиться компенсации расстройства, улучшить физическое и интеллектуальное развитие.
При среднетяжелом и тяжелом характере перивентрикулярной лейкомаляции малыш не будет соответствовать усредненным возрастным нормам – родителям следует быть к этому готовыми. Он позже начнет переворачиваться, присаживаться, ходить.
Затруднено и речевое развитие – слоги появятся позднее, предложения же будут практически недоступны. Иные проявления перивентрикулярной патологии:

- отсутствие естественного детского любопытства;
- болезненность и напряженность мышц конечностей;
- беспокойность, чрезмерная плаксивость;
- нарушение сна – прерывистость, частая путаность дня с ночью;
- грудное вскармливание затруднено – плохо выражен сосательный, а также глотательный рефлекс;
- отклонения в дательной системе – потребность в применении аппарата искусственного дыхания.
Легкая перивентрикулярная лейкомаляция компенсируется к школьному возрасту, при благоприятном течении патологии подросток ничем не отличим от сверстников. Тогда как при тяжелой форме болезни дети становятся инвалидами и требуют постоянного постороннего ухода.
Тактика лечения
Поскольку очаги лейкомаляции подразумевают необратимую гибель нервных клеток, то каких-либо четких схем устранения подобных перивентрикулярных состояний не разработано. Специалисты придерживаются симптоматического подхода – лечение направлено на уменьшение выраженности негативных проявлений.

Перивентрикулярная лейкомаляция у недоношенных детей требует незамедлительного принятия мер по улучшению снабжения клеток кислородом. Для этого следует восстановить полноценный кровоток. Эффективные группы медикаментов:
- ноотропы – усиливают приток крови к нервным клеткам: Пирацетам;
- противосудорожные средства – Карбамазепин;
- витаминные комплексы;
- при высоком внутричерепном давлении – Диакарб;
- при повышенной плаксивости, нарушении сна – успокоительные лекарства на растительной основе, к примеру, Валериана, Мелисса.
Помимо медикаментозной терапии, врачи рекомендуют курсы лечебного массажа и физиотерапии. Обязательно проводятся коррекционные занятия с психологом, педагогами – для стимулирования памяти, мышления, внимания, а также речи.
Родители детей с перивентрикулярной лейкомаляцией должны понимать, что чем больше внимания и труда они вложат в ребенка с первых же дней его жизни, тем лучше он будет развиваться. Поэтому все рекомендации врачей следует выполнять – прием лекарств и массаж, физкультура и правильное питание.
При тяжелой степени перивентрикулярной болезни лечебные мероприятия будут проводиться в стационарных условиях – восстановление дыхательной, сердечнососудистой деятельности, компенсация внутричерепной гипертензии. В этом случае о благоприятном прогнозе речи уже вестись не будет.

Профилактика
Крепкое здоровье детей – это результат усилий их мам с первых дней, когда они узнали о своей беременности. Для того чтобы перивентрикулярная лейкомаляция не возникала, рекомендуется заранее принимать меры профилактики:
- соблюдать принципы здоровой жизни еще на этапе планирования беременности;
- придерживаться сбалансированного питания, с присутствием в рационе различных овощей и фруктов;
- отказаться от всех вредных привычек, особенно употребления табачной и алкогольной продукции;
- заранее пройти консультацию врача, сдать анализы на присутствие в организме скрытых инфекций;
- избегать тяжелых физических, психоэмоциональных нагрузок;
- укреплять защитные барьеры – принимать витаминные комплексы;
- хорошо высыпаться;
- свести к минимуму контакты с людьми, страдающими от заболеваний инфекционного характера.

Узнавшей о своей беременности женщине следует незамедлительно встать на учет к врачу, который будет ее наблюдать на всех этапах внутриутробного развития малыша. Профилактике различных патологий, в том числе и периветрикулярной лейкомаляции у новорожденных, специалистами системы здравоохранения уделяется огромное внимание – разработаны стандарты профилактических исследований у беременных.
Крепкий, здоровый малыш – гордость родителей. Для его полноценного роста и развития – без лейкомаляции, будущая мать должна тесно сотрудничать с врачами и выполнять все их рекомендации.
Источник
Перивентрикулярная лейкомаляция (ПВЛ) у новорожденного — классификация, причиныНаиболее распространенным гипоксически-ишемическим повреждением у недоношенных новорожденных является перивентрикулярная лейкомаляция (ПВЛ). Miller et al. (2000) сообщали об этом состоянии у доношенных детей. Термин ввели Banker и Larroche в 1962 г. в отношении размягчения (malacia) белого (leicos) вещества. Большинство детей в их исследовании были рождены после 28 недели гестации и на момент смерти были в возрасте нескольких недель. Аноксические эпизоды были зарегистрированы во всех случаях. При патологоанатомическом исследовании встречались двусторонние, хотя необязательно симметричные, коагуляционные некрозы, примыкающие к наружному углу боковых желудочков. В последние годы классическая картина распознается реже и в работе Paneth et al. (1990) только 3 из 15 новорожденных с некрозами белого вещества имели классические изменения при ПВЛ. В настоящее время (Volpe, 2008) принято различать преимущественно очаговый тип повреждения белого вещества — с кистозными образованиями, ограниченными областью угла и затылочным рогом, вовлекающими в процесс зрительную лучистость, иногда распространяясь кпереди в область лобно-теменного белого вещества, и более диффузный тип, который сейчас чаще называют лейкоэнцефалопатией или повреждением перивентрикулярного белого вещества (periventricular white matter injury — PWMI), реже — ПВЛ (Leviton и Gilles, 1984, Back, 2006). В то время как эволюция в кисты, хорошо различимые при ультразвуковом сканировании черепа, является отличительным признаком очагового типа, более диффузные изменения интенсивности сигнала МРТ являются информативным показателем для диагностики диффузных патологических изменений белого вещества (Counsell et al, 2003). Кистозная перивентрикулярная лейкомаляция (к-ПВЛ) была впервые диагностирована с использованием краниальной ультрасонографии в 1982 г. (Hill et al., 1982а). По данным прежних патологических исследований, примерно 25% повреждений носили геморрагический характер (Levene et al., 1983). Как было отмечено, заболеваемость к-ПВЛ за последнее десятилетие снизилась (Hamrick et al., 2004) с 5-10% до менее 1% в некоторых центрах.
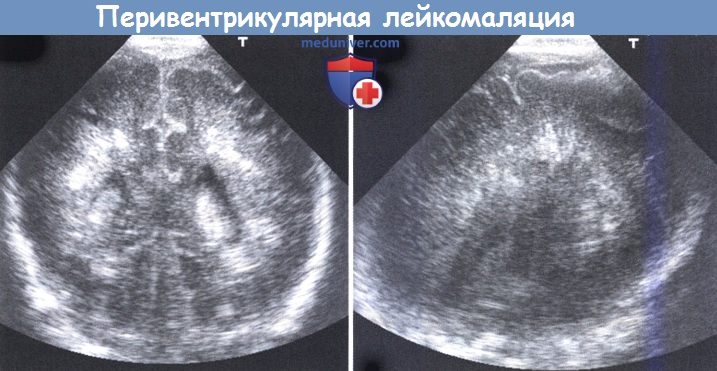
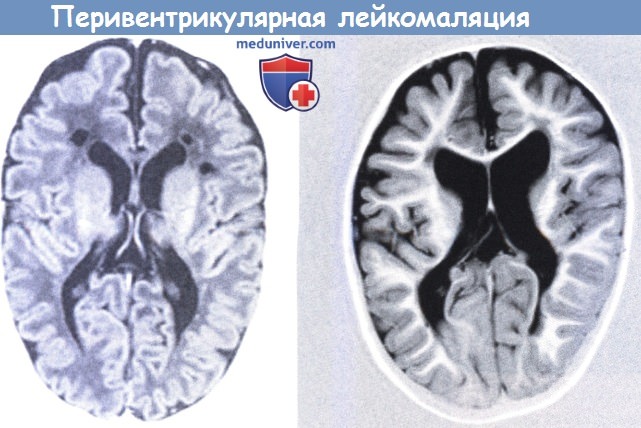
а) Сопоставления с нейровизуализацией. Начальные изменения, видимые при ультразвуковом исследовании, представляют собой участки повышенной перивентрикулярной эхогенности (ПВЭ), которые относятся к очень субъективным находкам. Некоторые предлагают измерять ПВЭ при сравнении их с эхогенностью сосудистого сплетения. Учитывается продолжительность ПВЭ, при длительном присутствии возрастает вероятность, что они указывают на среднюю степень ПВЛ. Кроме того, может помочь определение гомогенности ПВЭ. В случаях неоднородности («пестрой» ПВЭ), наиболее вероятно повреждение белого вещества, а пестрые участки чаще коррелируют с небольшими петехиальными кровоизлияниями на MPT (Sie et al, 2000b, Childs et al, 2001). ПВЛ можно разделить на 4 подгруппы (de Vries et al, 1992a). Стадия I дополнительно может быть разделена на две подгруппы, (а) гомогенные, и (б) негомогенные (пестрые) перивентрикулярные эхогенности (ПВЭ). Несколько исследований с применением МРТ показали, что имеется невыраженная корреляция между перивентрикулярной эхогенности (ПВЭ) и изменениями интенсивности сигнала в белом веществе (Maalouf et al., 2001, Debillon et al., 2003, Miller et al., 2003, Inder et al, 2003a). Раннюю ПВЭ можно было бы соотнести с диффузным сигналом сверхвысокой интенсивности (Diffuse excessive high signal intensity—DEHSI), который выявляется на Т2-взвешенных спин-эхо последовательностях у 70% недоношенных детей в приблизительном эквиваленте зрелого возраста. Измерение коэффициента диффузии (the apparent diffusion coefficient — ADC) подтвердило, что этот показатель действительно отражает повреждение белого вещества (Counsell et al., 2003). У небольшого количества младенцев очаги перивентрикулярной эхогенности (ПВЭ) постепенно превратились в локализованные или более обширные кисты. Чем меньше и чем более ограниченна киста, тем больше времени требуется для ее развития. Мелкие кисты могут остаться не выявленными. Более 50% небольших кист впервые выявляли при еженедельном ультразвуковом исследовании после 28 дней (Pierrat et al., 2001, de Vries et al., 2004). Более чем у половины детей маленькие кисты разрешались к 40 неделям постконцептуального возраста, приводя к легкому расширению желудочков (вентрикуломегалии) в некоторых, но не во всех случаях. С уменьшением длительности вентиляции новорожденных и возрастанием числа пациентов большинство младенцев переводят в районные стационары до развития кистозных изменений и возвращают для наблюдения в клинику в 40 и более недель постконцептуального возраста. Если ультразвуковое исследование не проводится в местных больницах, кисты могут оставаться не диагностированными, что, вероятно, является основной причиной плохой репутации краниального УЗИ как предиктора церебрального паралича (de Vries et al., 2004). В улучшении наблюдения за детьми группы риска по развитию кист МРТ, как было показано, может быть перспективным. Inder et al. (1999b) впервые продемонстрировали обширные изменения на ДВ-МРТ, предшествовавшие развитию кист. Получены немногисленные данные об очень ограниченном количестве детей с ПВЭ, обследованных на ранней стадии этого тяжелого расстройства (Bozzao et al., 2003). Кисты, даже обширные, могут разрешаться от нескольких недель до месяцев, и МРТ играет главную роль в определении распространенности повреждений белого вещества на этапе позднего неонатального периода. Классическая картина в периоде младенчества может быть представлена в виде неравномерного расширения боковых желудочков, различной степени утраты белого вещества, извилин, прилегающих к желудочковым стенкам, задержки миелинизации и перивентрикулярного глиоза (Byrne et al., 1990, Truwit et al., 1992). de Vries et al. (1993) обнаружили хорошую степень корреляции между тяжестью патологии при ультразвуковом исследовании новорожденных и глиозными изменениями на МРТ, в период младенчества. Современные технологии, использующие диффузионо-тензорное изображение (ДТИ), позволяют выполнить диффузионнотензорную трактографию (ДТТ) и таким образом отображать и подсчитывать белое вещество пирамидального тракта недоношенных новорожденных (Miller et al., 2002, Berman et al., 2005, Partridge et al., 2005). Counsell et al. (2006) указали на существенно повышенный радиальный коэффициент диффузии в задней части внутренней капсулы и утолщении мозолистого тела, а также значительно повышенный радиальный и аксиальный коэффициент диффузии в белом веществе семиовального центра, в белом веществе лобной, перивентрикулярной и затылочной областей. Эти данные, полученные Counsell et al. (2006), позволяют предположить, что DEHSI при стандартном МРТ отражает патологические изменения олигодендроцитов и/или аксонов белого вещества.
б) Патогенез. Патогенез ПВЛ многофакторный и менее понятен, чем при кровоизлиянии в герминативный матрикс и внутрижелудочковом кровоизлиянии (КГМ-ВЖК). Первоначально это состояние связывали с гипоперфузией пограничных зон в белом веществе, но исследования с использованием непрерывного измерения кровяного давления до сих пор не в состоянии определить гипотензию как независимый фактор риска для повреждения белого вещества (Trounce et al., 1988, Watkins et al., 1989, Dammann et al., 2002). Тяжелая гипокапния, которая приводит к снижению мозгового кровотока, в нескольких исследованиях была выделена в качестве самостоятельного фактора риска для развития ПВЛ (Calvert et al., 1987, Greisen et al., 1987, Graziani et al., 1992, Fujimoto et al., 1994, Wiswell et al., 1996, Okumura et al., 2001, Shankaran et al., 2006). У детей с развитием ПВЛ было обнаружено заметное снижение как мозгового кровотока, так и доставки кислорода к мозгу (Pryds, 1994). Результаты ближней инфракрасной спектроскопии (БИС), Tsuji et al. (2000) подтвердили дисфункцию церебральной ауторегуляции у 17 из 32 недоношенных детей; у 9 из них развились тяжелые внутричерепные повреждения по сравнению только с 2 из 15 с неизмененной ауторегуляцией. В нескольких интересных исследованиях была обнаружена связь между восходящей внутриматочной инфекцией, продукцией воспалительных цитокинов и повреждением белого вещества (Leviton и Gilles, 1984, Bejar et al., 1988, Murphy etal., 1995, Perlman et al., 1996, Verma et al., 1997, Yoon et al., 1997, Minagawa et al., 2002). В недавнем обзоре (Leviton et al., 2005) выдвинута гипотеза, что поражение белого вещества возникает в результате взаимного усиления врожденной и приобретенной иммунных систем. При мета-анализе была установлена связь между хориоамнионитом и церебральным параличом, и хориоамнионит был выделен в качестве фактора риска как для церебрального паралича (КР 1,9; 95% ДИ 1,5-2,5), так и для ПВЛ (КР 2,6; 95% ДИ 1,7-3,9) (Wu и Colford, 2000). Yanowitz et al. (2002) смогли показать взаимосвязь между хориоамнионитом, повышенным уровнем ИЛ-1 р и ИЛ-6, а также снижением среднего и диастолического давления крови после рождения. Уязвимость также зависит от степени зрелости белого вещества, называемой Back et al. (2001) «окном уязвимости развития». Они предположили важность гипоксически-ишемического/токсического повреждения метаболически активной олигодендроглии (Oka et al., 1993). На пике развития ПВЛ преимущественно представлены поздние предшественники олигодендроцитов. Кроме этого, Oka et al. указывали на то, что глютамат чрезвычайно токсичен в отношении дифференцирующейся олигодендроглии. — Также рекомендуем «Клиника и профилактика перивентрикулярной лейкомаляции (ПВЛ) у новорожденного» Редактор: Искандер Милевски. Дата публикации: 25.11.2018 |
Источник